用合成材料改造细胞环境一直是生物医学研究的长期挑战[ 1 ]。在实验室中设计新组织、鼓励受损组织的自我再生、用合成材料替换受损组织或进一步了解细胞过程的愿望都涉及细胞与人造材料(如植入物、支架、生物医学设备和细胞培养表面。这些材料经常遇到的设计元素是模仿自然细胞环境的一个或多个特征,其中细胞粘附和存活是主要考虑因素,此外还有更具体的方面,例如增殖、迁移或分化[ 2]。在自然界中,这些细胞反应受到细胞环境的影响[ 3 ];对于固体生物材料(即不包括水凝胶和细胞进入材料的类似生物材料),材料的表面特性定义了细胞与材料相互作用的性质[4 ]。
自然细胞环境高度复杂和动态[ 5-8 ],使其理解和模拟成为相当大的挑战。人们已经认识到,仅通过材料表面呈现与天然细胞外基质 (ECM) 中相似的特性(化学、形貌、刚度)不足以解决当前生物材料和医疗保健研究中的挑战 [5 , 6 ]。为了更好地了解细胞与材料的相互作用并开发用于再生医学应用的生物材料,必须将动态元素纳入生物界面中。
换句话说,响应材料,即在受到刺激时改变其一种或多种特性的材料,继续引起人们的广泛关注;大力开发新型刺激响应材料和表面,增强对材料响应的控制和变化;该领域进展的概述可以在近的一些评论中找到[ 7 , 9-16 ]。这些评论大多数讨论响应性材料,很少关注响应性表面和界面[ 14-16 ]。
本综述旨在概述设计新一代响应性细胞-材料界面(生物界面)所需的设计特征和挑战,并重点介绍该领域的当前策略和新进展。
细胞-材料相互作用
为了能够用人造材料模拟自然细胞环境的特性,先有必要了解细胞与其局部环境的相互作用。这包括天然细胞环境和人造材料与活细胞接触时产生的合成生物界面。因此,在讨论生物界面的设计和工程之前,先对细胞与其周围环境的相互作用进行简短的总结。虽然远程生物相互作用(例如神经元网络)具有很高的生物学重要性,但在生物界面的背景下,我们将重点关注细胞与其局部环境的相互作用。
细胞环境
细胞与其自然环境的相互作用是高度复杂和动态的,涉及许多相互关联的信号通路[ 3,5,8 ]。为了模拟这些相互作用的一部分,必须了解自然细胞环境的组成和特性以及细胞与其周围环境之间的通信途径。
ECM 组成和相互作用
细胞的环境是异构且动态的。它由大量蛋白质(形成 ECM)和介导相邻细胞之间相互作用的自由扩散分子组成。
细胞与其局部环境的相互作用对于组织的凝聚力和结构至关重要,并影响扩散、迁移、增殖和分化等细胞过程[17 ]]。细胞通过细胞膜中存在的蛋白质和碳水化合物以及通过例如胞吐作用将可溶性因子分泌到细胞外环境中与ECM和其他细胞相互作用。虽然涉及膜结合分子的相互作用仅限于细胞的直接周围环境,但分泌的可溶性因子可能与局部和更广泛的细胞环境相互作用。邻近细胞间相互作用由细胞连接蛋白(例如肝配蛋白和钙粘蛋白)介导,这些蛋白参与细胞间粘附、信号转导和细胞间的机械耦合[18 , 19 ]。
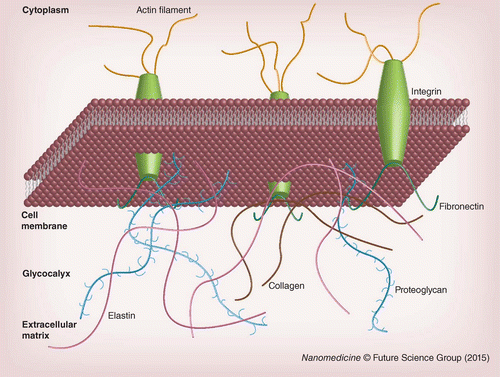
ECM 是一种复杂的基于蛋白质的水凝胶。构成 ECM 的一些主要组件如图 1底部所示。ECM 的主要成分是胶原蛋白,这是一种多样化的蛋白质家族,其螺旋原纤维为其他蛋白质提供结构支撑和结合位点 [ 20 ]。通过形成弹性纤维,弹性蛋白为 ECM 提供弹性和结构支撑 [ 21 ]。纤连蛋白、玻连蛋白和层粘连蛋白等蛋白质显示出其他蛋白质的结合位点,包括来自细胞膜的生长因子和粘附分子 [ 20 , 22 ]。
细胞与 ECM 的相互作用是由膜受体介导的。一类此类受体是整合素(见图1),是由 α 和 β 亚基组成的异二聚体膜蛋白,其特定配对决定了整合素与 ECM 蛋白呈递的配体的亲和力 [ 23 ]。研究多的 ECM 配体之一是次在纤连蛋白中发现的肽序列 RGD [ 24 ]。虽然 RGD 可能是的整联蛋白结合基序,但其他整联蛋白结合肽也已被报道,其中包括纤连蛋白中的 PHSRN、REDV 和 LDV 以及层粘连蛋白中的 IKVAV、YIGSR 和 PDSGR [19 ]。
除了膜蛋白之外,膜结合的碳水化合物缀合物也有助于细胞与其周围环境的相互作用。细胞膜中的碳水化合物结合物(糖蛋白、糖脂和蛋白多糖)在细胞外部糖萼周围形成一层不同成分和厚度的层,如图1所示的蛋白多糖所示[ 25 ]。通过这些膜结合的碳水化合物,细胞能够与其他细胞和 ECM 建立连接。
ECM 成分和结构的动态变化会影响 ECM 的空间和时间化学和物理特性 [ 3 ]。ECM 呈现的官能团类型、ECM 的拓扑结构和机械性能的变化可能导致细胞粘附和其他细胞过程的改变 [7 ]。这种动态行为是生物系统功能的一个组成部分,是干细胞分化和细胞迁移等重要生物过程的基础[ 26-28 ],以及疾病的发展[ 7 ]。
细胞不仅会对环境提供的线索作出反应,还会积地重塑环境[ 3 ]。通过胞吐作用和其他途径,细胞分泌重塑 ECM 并与其他细胞相互作用的分子。突出的例子是基质金属蛋白酶 (MMP),这是一种通过蛋白水解降解 ECM 的细胞分泌酶 [ 29 ]。其他细胞分泌的蛋白质,如胶原蛋白和纤连蛋白,有助于 ECM 的构建,从而影响 ECM 的结构和组成 [ 30 ]。
细胞粘附
粘附依赖性细胞依靠细胞粘附的形成(细胞将自身锚定到周围环境的机制)来生存和发挥功能。了解细胞粘附如何形成并介导细胞与其环境之间的通讯对于设计和工程功能生物界面至关重要。应该指出的是,大多数关于细胞粘附形成的见解都源于对 2D 表面的研究。有人提出,细胞粘附的作用在 3D 细胞培养环境中是不同的 [ 31 ]。
细胞粘附的形成被描述为四个不同的阶段:表面识别阶段;早期依恋阶段;中间附着阶段和晚期粘附或细胞扩散阶段[ 6 ]。这些终导致成熟粘附(称为粘着斑的分子复合物)的形成,整合素通过该粘附在细胞与其周围环境之间建立连接。这些过程是动态且可逆的。例如,细胞迁移需要控制粘着斑复合物的组装和分解,以使细胞能够与其周围环境形成和破坏粘附[ 32 , 33 ]。
整合素分子的细胞质成分通过中间蛋白(例如talin)与肌动蛋白细胞骨架连接[ 34 ]。因此,焦点粘附复合物有助于细胞-材料相互作用的形成和调节,并将有关机械、化学和地形线索的信息从细胞外环境翻译到细胞内环境[35 ]。细胞骨架的特性影响重要的细胞过程,例如弹性、迁移、分裂和分化。细胞骨架和局部细胞环境之间的粘着斑介导的连接提供了细胞和ECM之间的直接联系[ 32 ]。
生物界面特性
将人造材料引入活的生物环境(无论是在体外作为细胞培养材料,还是在体内作为生物医学植入物和设备)都会改变细胞环境,从而影响细胞功能和过程。再生医学采用多种人造材料,如金属、聚合物、陶瓷和玻璃[ 9 ];针对特定应用选择合适材料的考虑因素必须包括本体和表面材料特性。在本上下文中仅考虑后者,因为材料的表面是与细胞的一个接触点,并且在确定生物反应中起着关键作用[4 ]。
当与活细胞接触时,材料表面迅速被蛋白质覆盖[ 4 ]。因此,细胞很少与材料表面直接相互作用,细胞与材料的相互作用通常由表面吸附的蛋白质层介导[ 36 , 37 ]。吸附在表面上的蛋白质层的组成和特性由多种因素决定,例如溶液蛋白质组成和浓度、蛋白质大小以及特定的蛋白质-表面相互作用[38 ]。在细胞粘附表面上,所得的蛋白质层通常包括细胞粘附促进蛋白,例如纤连蛋白、玻连蛋白、层粘连蛋白和纤维蛋白原[ 36 ]。
由于细胞对表面的反应很大程度上取决于表面吸附蛋白质的特性(例如类型、浓度、分布和运动性),[30, 39] 基质表面特性的改变 [ 36 , 40–42 ]会影响其性质蛋白质层,从而控制细胞对生物材料的反应[ 43 , 44 ]。三种表面特性已被确定为细胞行为和细胞命运的主要决定因素:表面化学、表面形貌和表面弹性或刚度[ 5]。后两者都是身体特征,因此在本次审查中将被归为一类。虽然我们将分别讨论这些表面特性,但它们并不相互排斥,它们的各种组合可能会产生协同或不同的生物反应。
化学
材料表面化学成分的变化已被证明会影响广泛的细胞特性,包括粘附[ 45-48 ]、扩散[ 46 , 49 ]、迁移[ 46 , 50 ]、增殖[ 51 ]和分化[ 51] –53 ]。细胞反应与特异性(例如,特定分子或分子结构)和非特异性(例如,亲水性/疏水性和电荷)表面化学性质有关。
非特异性化学性质,如电荷[ 46 ]和润湿性[ 46 , 54 ]已被证明会影响细胞粘附[ 55 ]或间充质干细胞的表型和功能[ 56 ]。由于细胞表面通常带负电荷[ 57 ],因此表面正电荷的存在通常会促进细胞粘附。同样,中等亲水性分子也倾向于促进细胞粘附到表面[ 55]。特别是,与其他官能团如羧基(带负电)、甲基(疏水)和羟基(中性和亲水)基团相比,含有胺官能团的表面上的细胞粘附已被证明有所增加[58 ]。
生物分子可以固定在表面上,以利用细胞表面配体与 ECM 的特定相互作用。固定化蛋白质(例如层粘连蛋白)、肽序列(例如RGD)和碳水化合物(例如半乳糖)已被用来控制细胞行为[ 47 , 59 ]。纤连蛋白衍生的肽序列 RGD 因促进整合素介导的细胞粘附到人造表面而受到特别关注 [ 60 ]。
身体的
表面形貌、粗糙度、图案尺寸和顺序等物理特性在引导细胞-材料界面处的细胞反应方面发挥着重要作用[ 6,34,61 ]。地形特征的尺寸至关重要,因为它们影响细胞检测和响应它们的能力[ 62 ]。与整个细胞尺寸相匹配的微米级特征可能不会被细胞表面受体识别[ 34 ],而与细胞受体大小相似的纳米级特征已被证明对细胞对细胞的反应有重大影响。表面[ 34 ]。例如,几十纳米深度的形貌特征会影响细胞粘附[ 63,64 ]和分化[ 65 ]。
影响细胞响应的不仅是特征尺寸,还包括特征尺寸。表面上纳米级特征的组织方式同样会影响细胞的命运。与相同尺寸的有序图案(正方形或六边形排列)相比,圆形凹坑(100 nm 深,120 nm 直径)的无序排列导致间充质干细胞的成骨细胞分化增加[61 ]。
除了表面形貌之外,材料的基质弹性(或刚度)已被认为是指导干细胞命运的另一种物理特性[ 66 ]。间充质干细胞的谱系被证明与材料硬度的变化相关。在具有特定硬度的材料上获得的分化细胞类型与相关组织的自然硬度相对应。
生物材料的进化
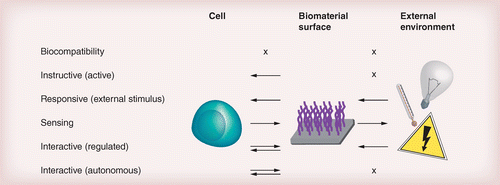
自 50 多年前生物材料研究出现以来,生物材料的定义和要求发生了很大变化 [ 9 , 67–68 ]。图 2显示了生物材料类别及其与细胞和外部环境的相互作用的列表。初,生物材料选择的重点是生物相容性,目标是完抑制或减少细胞与材料的相互作用,以尽量减少细胞或组织对材料的不良反应(例如毒性、炎症)[69 ]。对细胞与材料相互作用的进一步了解导致了生物活性(或指导性)生物材料的设计,这些材料与宿主组织结合并积增强材料整合[ 70]。对提高生物材料性能和更紧密地模拟 ECM 内动态过程的持续需求导致了响应性生物材料(也称为智能生物材料)的出现,它们能够动态地(在某些情况下可逆地)改变其特性外部刺激的存在[ 9 , 11 ]。在这种情况下,信息流从环境通过材料到达细胞。虽然不是本次审查的一部分,但应该指出的是,逆过程(即由材料收集有关细胞的信息并转换到外部处理单元)代表了传感设备中的过程。
尽管现代生物材料的功能性和复杂性不断增加,但当前的技术仍然无法模拟自然细胞环境错综复杂的相互作用。ECM 不仅向细胞提供信号,还对细胞做出反应,例如通过酶催化 ECM 降解 [ 29 , 30 ]。相比之下,迄今为止大多数生物材料都是细胞指导性的,换句话说,它们旨在引发细胞特定的所需反应,从而控制细胞过程[6 ]。在一项具有里程碑意义的研究中,使用合成聚合物水凝胶模拟了 ECM 的酶反应性,该水凝胶通过酶可裂解的肽序列进行交联 [ 71]。该聚合物水凝胶被证明对细胞分泌的酶敏感,从而建立了细胞响应性生物材料的概念。随后,在 2D 表面上也实现了酶响应性 [ 72 , 73 ],从而导致了对细胞分泌的磷酸酶做出响应的肽表面的发展 [ 74]]。这为交互式生物材料铺平了道路,其中材料和细胞都能够动态响应各自其他系统呈现的刺激。对于交互界面的设计,我们区分了两种类型的界面,分别标记为外部监管和自主。如果外部刺激能够或确实需要控制界面相互作用,则该界面是外部调节的。相比之下,自主接口能够完自我维持且立于外部因素来执行其功能。
越来越明显的是,下一代生物材料应包括与周围细胞相互作用的重要元素,通过人造材料与生物周围环境的更无缝集成来提供增强的生物材料功能。虽然散装材料的这种开发已经开始,但能够提供交互式细胞-材料界面(交互式生物材料)的生物响应表面的设计将带来重大挑战和机遇。
设计响应性生物界面
制造响应性生物界面必须考虑三个主要材料特性。这些由图 2中的三个组件表示。先,材料必须以动态方式引发预定的生物反应。其次,材料的生物反应必须与材料表面特性的可控变化相关。三,这些动态表面特性必须以预定义的方式响应特定的刺激。这三种表面特性必须因果联系起来,以产生从刺激触发表面特性变化到诱导差异生物反应的一系列事件。终,这些事件旨在模仿自然生物过程的动态元素[ 8,75 ]。
生物反应
从生物学角度来看,参与生物界面生成的材料表面必须提供化学和物理线索,以促进一般和特定的生物反应,不一定同时发生,而是以时间或空间受控的方式发生。
与生物相容性和生物活性材料一样,响应性生物界面必须是无毒的,并且在表面可以采用的至少一种材料状态下支持细胞粘附和存活。许多生物相容性材料,包括胶原蛋白、藻酸盐、聚乙醇酸、聚乳酸和聚乳酸-乙醇酸共聚物是已知的,并已被美国 FDA 批准用于临床应用 [ 76 ] 和许多其他材料用于生物医学研究,以研究细胞与材料的相互作用并开发新的生物医学材料。
除了一般材料特性外,材料表面特性还必须能够适应两种不同的状态,从而引起不同的细胞反应,通过改变人工细胞环境在特定时间或空间点的特性来有效地模拟细胞外环境[ 8 ]。对各种细胞反应的动态控制将是可取的。控制表面上的细胞粘附和/或存活可用于帮助生物材料整合到活体组织中[ 77 ],分离实验室细胞培养物以进行进一步处理[ 78 ],或控制空间细胞组织以创建更复杂的人造组织[ 79]]。受刺激的细胞迁移和化也可能有助于设计更复杂的组织结构,并控制细胞多孔 3D 物体的数量。通过在体外重建干细胞生态位来控制干细胞命运(包括增殖和分化)的材料是开发干细胞疗法的主要兴趣[ 5 ]。材料表面与许多其他细胞过程(包括细胞分裂、细胞间通讯和代谢过程)的测量、控制和相互作用可能会在未来的生物技术和生物医学领域产生有趣的应用。
材料反应
为了在相同的生物界面环境中呈现具有不同生物特性的表面,材料表面必须能够响应刺激的存在而改变其一些物理或化学特性。这些动态表面变化以依赖于时间的方式发生,但还可能受到空间限制。
刺激引起的材料变化可以通过改变材料表面的电离状态或形态来影响一般表面特性,例如润湿性[ 80-82 ]或电荷[ 83 ]。为了模拟 ECM 中细胞粘附受体配体等生物分子显示的动态变化并调节更具体的细胞-材料相互作用,材料表面上生物分子的呈现也可能会因刺激而变化[72 , 84–87 ] ]。后,为了模仿 ECM 动态改变其结构的能力,需要具有刺激引起的形貌和弹性变化的表面 [ 88-91 ]。
复杂生物环境中的稳定性是另一个重要方面,如果要建立长期生物界面,则至关重要[ 37 ]。随着时间的推移,酶降解、非特异性水解、蛋白质吸附和其他生物过程可能会影响表面的稳定性和性能。必须调整材料表面承受这些影响的能力,以匹配预期的生物应用。
刺激
为了能够控制材料和细胞反应,材料表面特性的变化必须与特定触发事件(即刺激)的存在相关联。适当刺激的选择取决于应用要求、将特定材料变化与特定刺激相匹配的能力以及材料/刺激相互作用的响应特征。
应用要求包括生物学和技术方面。从技术角度来看,刺激必须能够物理到达界面并与之交互。虽然这对于体外应用可能并不重要,但在体内应用中,界面可能深埋在活体组织内,可能无法轻松访问界面以进行外部控制刺激[ 15 ]。从生物学角度来看,刺激必须被细胞耐受,并且不能直接触发细胞本身的反应。因此,理想的刺激不应显着改变细胞环境的生理条件[ 92]。生物系统中的选刺激是光、电势、较小的 pH 或温度变化以及机械应力 [ 93 ]。这些刺激通常是从外部施加的,换句话说,它们不是界面系统本身的一部分。对于具有交互性和潜在自主性的新一代生物材料,生物分子越来越多地被使用,目的是开发不需要添加外部刺激的细胞响应材料[94 ]。
为了实现特定的、有针对性的交互,材料响应必须与特定的触发事件相匹配,并避免对其他因素的非特定材料响应。非自然的、外部施加的刺激,例如特定波长的光[ 95 ]和电化学势[ 96 ],可以与特定的材料响应专门匹配,而用作刺激的生物分子预计不太具体。细胞环境多样化,能够提供可以触发材料反应的生物分子[ 97]。虽然这为设计细胞响应性生物界面提供了机会,但它也带来了挑战,因为生物分子响应性材料的响应可能不如其他响应性生物界面那么具体。特别是,酶[ 98 ](例如蛋白酶)可能会导致基于肽的界面的不良反应或降解[ 37 ]。
材料对刺激的反应特性是多种多样的;刺激暴露时间、材料响应的开/关时间和响应的可逆性决定了响应生物界面的性能[ 99 ]。材料属性切换的速度取决于提供刺激的速度以及材料对这些变化的响应速度(开/关时间)。一些刺激(例如光)可提供快的曝光时间,但可能会受到表面分子重排速度的限制 [ 100]。对于不可逆的刺激反应(例如,光解或酶促降解),仅需要考虑“开启”响应时间。对于可逆材料,原则上有两种情况:持续响应,其中表面变化仅在刺激(例如 pH 或温度)存在期间持续存在;以及响应,即使在刺激(例如,酶)存在后也持续存在。和电化学势)已被删除。这些差异可能并不总是严格适用,因为即使没有任何额外的刺激,某些材料(例如光响应分子(例如偶氮苯和螺吡喃))也可能在较长时间内自发转变回热力学稳定状态[101 , 102 ]。
后,刺激的作用可以是普遍的,影响整个界面,也可以局部限制在材料的特定区域。刺激的性质通常决定其影响的范围。如果将环境中的一般变化(例如pH和温度)用作触发事件,则定位通常是不可能的。其他可溶性因子(即生物分子)也很难在空间上聚焦。微流体装置和电阵列提供了在适度局部范围内操作某些刺激暴露事件的策略[ 103 , 104 ]。利用光可以实现刺激应用的高空间分辨率[ 95 ]。
刺激的选择很重要,因为它对响应界面属性的各个方面施加了特定的约束;因此,所选择的刺激必须与预期应用很好地匹配。
工程响应生物界面
虽然许多具有动态化学或物理特性的表面已经使用多种不同的材料和刺激进行了描述,但我们将在这里将我们的兴趣限制在那些已经或可能用作响应性生物界面中的表面的表面。在讨论使用这些刺激实现的生物学相关材料表面响应之前,我们将重点介绍已使用并发现与细胞环境兼容的刺激。后,将提供通过响应表面控制的生物特性的简短总结。
刺激
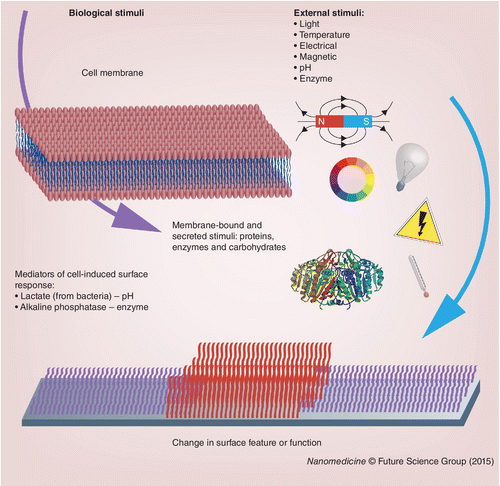
为了通过人造生物界面实现定义细胞和 ECM 之间自然相互作用的交互质量,不仅需要控制材料表面对刺激的响应方式,而且还必须仔细设计和整合刺激机制本身进入界面。已有几篇综合综述讨论了用于设计响应性材料和表面的刺激类型 [ 7 , 9–16 ]。在这里,我们将简要讨论迄今为止在刺激起源的背景下设计响应性生物界面的刺激,如图 3所示,因为这决定了材料在再生医学中的应用范围。
外部刺激
在本文中,外部刺激将被定义为源自生物界面环境外部、由与生物系统分离的更广泛环境中的事件产生的刺激。由于这包括易于由人或机器控制的信号,因此这是迄今为止触发表面响应的普遍的方式。图3显示了外部刺激的表示;人工改变温度[ 80 , 89–90 ],施加电势[ 83 , 105–107 ],光[ 85–86 , 108–109 ]和机械力[ 91 , 110 ]]都被用来触发化学或物理表面特性的动态变化,从而影响细胞的行为。此外,生物环境中自然存在的生物分子——例如酶[ 72 , 74 ]和碳水化合物[ 87 ]——已被人为添加到系统中以触发生物界面的响应。
用于生物界面的热响应材料通常是聚合物,其聚合物链与溶剂(例如水)的混溶性随温度变化。温度的变化导致材料[ 111、112 ]的水合状态的变化。如果用作表面薄膜,这将影响聚合物薄膜的润湿性和形态。温度响应材料的典型例子是聚(N-异丙基丙烯酰胺)(PNIPAM)[ 113 ]和弹性蛋白衍生的多肽[ 114 ]。其他材料如聚(ε-己内酯)被用作形状记忆材料来制备具有动态变化的形貌特征的表面[ 89 ]。
pH响应生物界面主要基于聚丙烯酸(PAA)和聚甲基丙烯酸(PMAA)[ 115 , 116 ]。它们的表面电荷和水含量会发生类似于热响应表面的变化。这些材料与高纵横比形貌特征的整合允许使用pH响应凝胶来可逆地调节表面形貌特征的方向[ 88 ]。在这些情况下,水凝胶的膨胀和收缩会对地形特征施加机械力,从而使它们受到机械应变,导致它们弯曲。
电势已更广泛地用于改变生物界面特性;它们的影响范围从表面分子构象的重组[ 83,96,106 ]到诱导调节表面化学基团存在的化学反应[ 107,117–119 ]。这些材料依赖于导电基底材料的存在。
光响应分子(例如偶氮苯)被纳入聚合物薄膜和自组装单层(SAM)中,以引起表面化学官能团的光响应重新取向[ 85 , 108 ]。偶氮苯的一种异构体与α-环糊精形成主客体复合物的能力也被利用,能够通过自组装过程将化学官能团可逆地附着到α-环糊精改性表面上[86 ]。
磁响应材料已被用来通过将磁性纳米粒子掺入聚合物水凝胶基质来改变细胞与表面的相互作用。施加磁场会导致水凝胶表面变形,从而导致水凝胶表面机械性能的改变[ 120 ]。
力响应生物界面由聚合物薄膜制备而成,可改变表面的孔隙率和形貌等物理特性。前者用于调节界面处生物分子的可用性[ 121 ],而后者可用于在表面上可逆地呈现地形图案[ 91 ]。
生物刺激
出于本目的,生物刺激被定义为可以由自然细胞环境提供的刺激。如图3所示,这些刺激可以是细胞分泌到其局部环境中的可溶性因子,也可以是固定在细胞膜上的分子。尽管由于技术原因,目前大多数生物刺激都是外部提供的,但它们确实提供了直接与细胞连接表面的潜力,并使它们能够动态响应生物环境的变化,从而更接近自主、交互式的设计细胞-材料界面。
众所周知,生物刺激可以影响散装材料的特性。值得注意的是,研究表明,含有肽作为交联剂的丙烯酸酯水凝胶可以被细胞分泌的 MMP 降解 [ 71 ]。近,一个证据表明细胞分泌的酶(即碱性磷酸酶)也可能改变磷酸化肽表面的特性[ 74 ]。作为具有高特异性和选择性作用的酶的替代方案,通过细胞介导的整体特性(pH)变化来触发表面响应也是可能的[122 ]。这些策略现在开辟了设计细胞响应生物界面的可能性,类似于现有的细胞响应散装材料。
生物分子响应表面已被制备成与碳水化合物、肽或酶相互作用。碳水化合物相互作用通常通过与表面结合的硼酸形成可逆键来发生[ 87 ],而肽已连接到通过非共价相互作用固定在表面上的互补肽链[ 84 , 123 ];在这两种情况下,刺激物(另一种碳水化合物或肽)的竞争性替代会导致化学表面成分的变化。核苷酸和碳水化合物响应材料已被证明可以调节表面的润湿性[ 81 , 82]。酶已被用来通过特定共价键的不可逆裂解来改变表面化学性质[ 72 , 74 ]。
材料反应
与影响细胞行为的主要表面特征类似,迄今为止纳入响应性生物界面的材料响应在这里被归类为化学或物理变化。后者包括地形和弹性的变化。
动态化学性质
表面化学是细胞与材料相互作用的主要决定因素。由于 ECM 向细胞呈现的化学物质不是静态的(例如,蛋白质组成、构象和结构会不断变化),因此能够动态调节细胞和人体之间界面上的生物相关化学信号。人造材料对于模仿生物行为很有吸引力。
通过改变表面润湿性和调节表面特定化学基团的可用性,获得了具有动态表面化学的生物界面。后者主要关注基于 RGD 的肽在表面的呈现,但也报道了一些其他生物分子的表面呈现的调节。表 1概述了此处讨论的诱导生物界面化学表面变化的策略。
润湿性
通过控制聚合物膜的水含量,可以以响应且可逆的方式改变表面的润湿性。pNIPAM 或 PMAA 等聚合物的溶胀程度(以及水含量)可以通过改变温度或 pH 等环境特性来改变 [ 80 , 122 ]。环境条件的变化会影响聚合物进行分子内相互作用的能力,从而调节聚合物膜内可吸收的水量[14 ]]。水含量的变化随后改变了聚合物表面的润湿性。这种刺激响应的表面润湿性可用于调节材料的细胞粘附特性,并在细胞片的制造中具有突出的用途[ 78 , 80 ]。
除了 pH 值和温度之外,生物分子也可用于改变聚合物表面的润湿性。使用多组分聚合物薄膜系统实现了表面润湿性从超疏水(水接触角为 150 °)到超亲水状态(水接触角为 0 ° )的可逆变化,该系统包含核苷酸响应性共聚物PNIPAM、苯基硫脲和苯基硼酸[ 81 ]或PNIPAM和3-(丙烯酰硫脲基)苯基硼酸的碳水化合物响应性共聚物[ 82 ]。
RGD的介绍
由于 RGD 在整合素介导的细胞粘附中的作用,基于 RGD 的肽在表面上呈现的动态变化引起了相当多的关注。因此,人们设计了大量的策略来制备响应性肽表面。对表面上肽展示的控制可以通过形成或破坏共价键、改变分子自组装或改变分子构象来原位完成。虽然共价键的变化通常会导致表面组成的不可逆变化,但自组装和构象诱导的表面变化通常是可逆的。下面,我们将回顾在表面上呈现基于 RGD 的肽所采用的策略,这些策略原则上也可用于其他短肽序列。
分离
使用电位作为刺激,可以实现基于 RGD 的肽从表面的分离。通过在细胞(成纤维细胞)存在的情况下向界面施加电势,可以实现 RGD 封端的烷硫醇从金和氧化铟锡表面的直接解吸 [105 , 107 ]。这导致从表面去除完整的硫醇-肽缀合物,导致单个细胞、球体和细胞片的分离。肽缀合物解吸的另一种方法是裂解肽和表面系链之间的氧化还原敏感连接体 [ 117 , 118]。通过施加电化学势,醌可以可逆地转化为氢醌。这些通过酯或甲硅烷基键带有肽的分子的衍生物可以被电化学诱导以断裂与肽的连接并将肽从表面释放,从表面去除细胞粘附配体并导致细胞脱离。
依恋
醌能够与环戊二烯发生狄尔斯-阿尔德反应,使得与环戊二烯缀合的肽可以在生理条件下固定在醌表面上。对于对苯二酚表面,可以根据需要通过电刺激触发该反应,导致对苯二酚氧化为醌[ 119 ]。这种方法用于动态改变图案表面的细胞粘附性。在用纤连蛋白(一种细胞粘附促进蛋白)图案化的表面上培养的成纤维细胞的粘附初被限制为蛋白质图案。原位通过电诱导醌形成激活周围表面,使得肽-环戊二烯缀合物能够在细胞存在的情况下附着,使整个表面细胞粘附并允许成纤维细胞填充整个表面[117 , 119 ]。尽管没有严格以刺激响应方式执行,但应该提到的是,使用类似的策略来控制表面上两种不同细胞类型(U2OS 和 RPE1 细胞)的位置[ 79]。在叠氮化物封端的表面上,为一种细胞类型的粘附创建了纤连蛋白图案。叠氮化物表面可以与环辛炔双环[6.1.0]壬炔-肽缀合物进行无催化剂环加成(点击反应),使剩余的表面细胞粘附并允许在空间上限定二个细胞系的培养。表面。
可逆共价结合
共价键的形成也可用于使用 RGD 序列可逆地修饰表面。碳水化合物中存在的二醇对硼酸具有高亲和力,并通过硼酸酯的可逆形成与硼酸结合。因此,含有与 RGD 基肽缀合的聚合物的碳水化合物可以固定在显示用苯基硼酸装饰的聚合物刷的表面上 [ 87 ]。该细胞粘附表面显示出支持 MG63 细胞的粘附,随后可以通过添加碳水化合物(葡萄糖或果糖)竞争性取代碳水化合物聚合物并从材料表面去除 RGD,从而将其从表面去除。
解锁
与通过响应刺激而连接或分离肽来改变表面上肽的量不同,还可以通过用共价结合的封闭基团掩蔽表面结合肽来调节表面结合肽的可用性。通过用空间庞大的芴甲氧羰基 (Fmoc) 基团终止肽,使细胞无法接近连接到玻璃表面的 PEG 链末端的基于 RGD 的肽序列 [72 ]。成骨细胞不会粘附在 Fmoc 终止的肽表面,但当通过酶促(弹性蛋白酶)切割末端丙氨酸-丙氨酸序列去除封闭基团时,RGD 序列变得可接近,并且细胞粘附成为可能。
通过自组装实现可翻转显示
迄今为止讨论的化学表面变化主要集中在共价键的修饰上,因此通常是不可逆的。使用精心设计的自组装材料可以设计具有可逆化学性质的表面。通过模拟蛋白质和天然肽参与形成超分子结构基序的特定非共价相互作用的能力,可以定制设计具有形成异二聚体复合物(所谓的拉链分子)的特定氨基酸序列的多肽。如果互补多肽拉链分子之一被 RGD 序列终止并附着到表面,则与二个拉链序列的二聚化能够实现表面化学的非共价、可逆调节 [ 84 , 123]。如果互补链与 PEG 链缀合,二聚化将导致表面的 RGD 序列被 PEG 掩蔽,使表面非细胞粘附并导致成纤维细胞脱离。通过添加未修饰的互补拉链序列(竞争性地取代 PEG 缀合物)可以恢复表面的细胞粘附性 [ 84 ]。
一种不同的自组装方法可逆地触发基于 RGD 的肽的展示,利用主客体化学,其中较小的分子嵌入较大的笼状分子中以形成超分子复合物。偶氮苯是一种光响应分子,在反式状态下能够参与与 α-环糊精的主客体相互作用;如果偶氮苯的构象改变为顺式状态(通过光照),所产生的构象变化会阻止偶氮苯进入α-环糊精中的空腔。通过将肽序列 GRGDS 与偶氮苯偶联,可以调节 α-环糊精表面响应光的化学功能化 [ 86 , 109]。当偶氮苯处于反式状态并附着在表面时,显示的 RGD 序列能够附着 HeLa 细胞。365 nm 的肽辐射会破坏超分子复合物,从表面去除肽序列并导致细胞脱离 [ 86 ]。
通过构象变化实现可逆显示
偶氮苯响应光而呈现两种不同异构形式的能力已被更广泛地利用来改变表面结合分子的构象,从而动态影响表面化学性质。基于 RGD 的肽的可用性可以通过调节其连接到表面的接头的长度来控制。因此,环状RGDfK通过偶氮苯连接体结合在聚甲基丙烯酸甲酯基表面上,并用光(366或450 nm)照射以引起偶氮苯连接体的光异构化并调节连接体长度[85 ]。这被证明可以有效控制 MC3T3 E1 小鼠成骨细胞的粘附。虽然这表明光调制肽展示可以影响细胞粘附,但并未进行表面转换在细胞存在的情况下原位进行。使用与刚刚讨论的类似的设计原理,基于 RGD 的肽可以通过中间偶氮苯部分连接到基于 PEG 的 SAM,并通过光照射调节 RGD 的显示[108 ]。在这项研究中,表明在成纤维细胞存在的情况下,表面的细胞粘附性可以可逆地原位改变。
通过向表面施加电势也可以引起构象表面变化以改变表面化学性质。结果表明,通过向表面施加电化学势,将 SAM 的带电端基吸引到基材表面,可以重新定向 SAM,从而改变电荷以及表面显示的化学功能[124 ]。该原理用于控制蛋白质(中性抗生物素蛋白)[ 96 ]和细菌(Marinobacter Hydrooclastus)[ 83]]附着到表面,特别是不是通过调节基于RGD的肽的展示,而是通过改变表面的电荷和/或亲水性。为了控制肽 (GRGDS) 在表面上的显示,在包含肽缀合物和带电荷端基(硫酸盐和叔胺)的分子的混合 SAM 中采用了相同的电化学控制机制 [106 ]。在没有电势的情况下,带电分子会延伸并保护肽免受在这些表面上培养的细胞的影响,从而防止细胞粘附。施加电势导致带电分子重新朝向表面,使肽可用于细胞相互作用并促进内皮细胞和分化的 HL60 细胞的粘附。
尽管本身不可逆,但应该注意的是,电化学势也可用于重复改变肽序列的环化。以羟胺封端的表面结合的肽序列可以与表面结合的氢醌进行电化学刺激的环化,类似于上面讨论的反应[ 125 ]。所得氧亚氨基醌的电化学还原导致环状结构打开。因此,该表面能够从线性肽结构转变为环状结构,然后再转换回线性肽结构,并且表明这些结构变化影响成纤维细胞的扩散和迁移。
其他生物分子的介绍
整合素在细胞粘附和细胞信号传导过程中的重要性无疑促进了以 RGD 作为生物界面特性化学修饰剂的动态表面的流行。在这里,我们将简短讨论对细胞过程调节至关重要的另外两种生物分子的可用性的控制;神经递质谷氨酸和碱性磷酸酶。
为了设计一种能够与生物对应物连接的人工突触,在电表面制备了基于聚吡咯的分子印迹聚合物,作为谷氨酸的储存库[126 ]。谷氨酸在生理条件下整体带负电荷;通过改变聚合物涂层电的静电势,谷氨酸盐可以根据需要动态释放并与聚合物结合。到目前为止,这种方法还处于概念阶段,尚未在与实际生物系统的接口中实现。
在自然界中,细胞持续控制酶的活性,例如,通过将酶分泌到细胞外空间或通过响应其他事件而抑制或激活酶。近的研究表明,表面固定的碱性磷酸酶的可用性可以根据机械刺激进行调节[ 121 ]。该酶被固定在由聚(l-赖氨酸)和透明质酸。该薄膜覆盖有一层聚(二烯丙基二甲基铵)和聚(4-苯乙烯磺酸钠),其在静止状态下对基材保持不渗透性,但在机械拉伸时变得多孔。因此,薄膜的拉伸提供了对酶可及性的控制,虽然这可能不是严格的界面相关系统,但它确实表现出类似于细胞与其环境相互作用所采用的基本生物过程的特征。
动态物理特性
现在已经确定,细胞外环境的地形和硬度的影响对于确定细胞如何与其周围环境相互作用至关重要。人们在设计 3D 结构(特别是水凝胶)方面投入了大量精力,以动态控制适合细胞培养的材料中的这些物理参数,从而提高我们确定细胞命运的能力。虽然这些块状水凝胶材料中的一些可以作为薄膜转移到其他基底上以产生生物界面,但具有原位可调节形貌和/或硬度的表面对于例如干细胞命运或神经元引导的体外控制是有吸引力的。表 2给出了下面讨论的方法的概述。
地形生成
细胞培养基质表面的凹槽已被广泛用于实现细胞的定向排列或迁移[ 12 ]。微米尺寸凹槽的可逆形成可以通过压缩支撑在聚二甲基硅氧烷(PDMS)上的氧化聚合物薄膜(Epo Tek,一种专有材料)来实现[91 ]。地形特征的形成导致C2C12成肌细胞沿着凹槽定向;值得注意的是,这种细胞方向是可逆的,在去除地形特征后,细胞再次采取随机方向。当间充质干细胞在具有可逆微米级凹槽拓扑的表面上培养时,观察到类似的效果[ 89]。这些材料是通过在聚(ε-己内酯)表面产生记忆形状效应来制备的。通过将材料暴露在 40°C 下 10 分钟,以热响应方式实现从一种形状到另一种形状的转变。原则上,导电聚合物薄膜已经证明了表面纳米尺寸形貌特征的可逆形成[ 127]]。借助原子力显微镜,将纳米尺寸特征写入电沉积聚联噻吩薄膜中。这些特征可以通过电化学氧化聚合物薄膜来平滑。随后吸收反离子(高氯酸盐)导致聚合物膜膨胀并使纳米压痕变得平滑。虽然这项工作尚未应用于生物学背景,但它证明了动态控制生物学相关尺寸的地形特征的可行性。
地形重新定向
修改表面上预先存在的地形特征的一种方法是根据刺激重新调整特征的方向。具有高纵横比形貌特征的表面(例如,直径远小于柱高度的柱)可以通过将形貌蚀刻到基板材料(例如,硅的环氧聚合物)中来制备[128 ]。通过将这些结构部分嵌入水凝胶中,使得特征的顶部从表面结合的水凝胶膜突出,水凝胶膨胀的变化可用于对柱施加机械力并使它们弯曲,从而重新定向结构的形貌特征表面 [ 129]。可以设想各种刺激来驱动这种拓扑结构的重新排列。值得注意的是,pH 响应型丙烯酸酯水凝胶已被证明能够在浸入水中时控制此类表面的微形貌[ 130 ]。此外,通过使用不对称的形貌结构或通过在表面的特定区域对水凝胶进行图案化,实现了表面微形貌的单向和局部限制的重新定向[88 , 130 ]。这些形貌变化是可逆且可重复的,并且通过仔细设计水凝胶膜来调节刺激反应的能力使其对于生物环境中的应用具有吸引力。
地形形状
上述用于形成或去除表面上的地形特征的记忆形状效应也可用于实现形状转变。通过先在交联过程中压印具有初级形状的聚(ε-己内酯)表面,然后在高温机械应变下压印次级形状,然后在应变下冷却,可以在同一表面内压印两个单的形貌[ 89 ] 。结果表明,该程序可用于在适合细胞培养的条件下在这两种微米大小的形状之间可逆地切换(例如,六边形和正方形之间或L形和圆形之间)。
地形和刚度
聚(ε-己内酯)的温度响应特性还可用于同时调节表面的整体刚度和形貌。通过改变聚合物薄膜内的交联程度,结果表明可以调节温度响应性,使得刚度/粗糙度转变发生在生物可接受的温度 (33°C) [ 90]。低于转变温度时,材料相对较硬(50 MPa)并显示出粗糙的表面;温度升高到 33°C 以上会降低刚度 (1 MPa),并产生光滑的表面形貌。结果表明,这种转变导致在聚(ε-己内酯)表面培养的成肌细胞呈现圆形形态并终从表面分离。相比之下,成纤维细胞对表面性质的物理变化的反应要弱得多,只有 20% 的细胞改变了其形态。
磁响应水凝胶是引发物理表面性质可逆转变的另一种方式。水凝胶中掺入的磁性颗粒(甲基丙烯酸 2-羟基乙酯、二甲基丙烯酸乙二醇酯和苯乙烯马来酸酐共聚物)如果置于磁场中,会使水凝胶表面变形。由于磁力作用在捕获的颗粒上,水凝胶受到机械应变,导致材料表面变形以及水凝胶刚度的变化。在这些水凝胶表面培养的间充质干细胞已被证明可以分化成软骨,以响应水凝胶物理特性的磁响应变化[ 120 ]。
生物反应
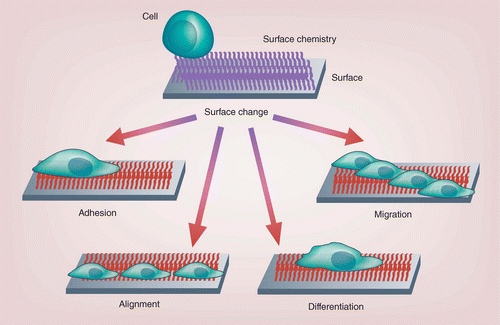
细胞以动态方式调节 ECM 并对其做出反应;ECM组成或结构的变化会对细胞粘附、迁移、分化和其他重要的细胞过程产生显着影响[ 3 ]。为了模拟这种相互作用,生物界面内的人造材料表面必须能够由于表面特性的物理或化学变化而引发有意义的生物反应。图 4中捕获了由于动态变化的表面特性而观察到的细胞响应,并将在以下部分中简要讨论。
据报道,响应性表面普遍的生物反应是细胞粘附的调节。通过动态改变基于RGD的肽在表面上的呈现,成骨细胞[ 72,85 ] 、成纤维细胞[ 84,105,107-108,110,123 ]、内皮细胞[ 106 ]和HeLa细胞[ 86,109 ]的粘附] 已经被报告了。在某些情况下,表面的细胞粘附性可以反复且可逆地改变[ 84-86、106、108-109、123 ]]。与旨在收获细胞片层的基于 pNIPAM 的热响应表面类似 [ 131 , 132 ],许多细胞粘附调节表面被提出作为收获细胞的替代途径。值得注意的其他应用集中于空间控制细胞粘附的能力,以便能够以预定义的模式共培养不同的细胞类型[ 79 ]。
在动态表面上实现的另一种生物反应是间充质干细胞[ 89 ]和成肌细胞[ 91 ]与动态微米尺寸的地形特征的对齐。细胞排列对于神经网络和肌肉等来说很重要;因此,界面处的可逆细胞排列作为生物界面致动器或支持组织的定向生长可能很有吸引力。
通过将材料暴露于磁场来改变表面形状和硬度后,在水凝胶表面上完成间充质干细胞向软骨的分化[ 120 ]。后,研究表明,成纤维细胞的扩散和迁移可以响应表面肽序列构象的动态变化而改变[ 125 ]。
显然,控制特定细胞反应的静态表面设计所取得的进展尚未转化为相同程度的动态表面。当我们了解哪些表面特性调节特定的生物反应时,有必要考虑如何将这些特性以动态方式纳入生物界面。这将使我们能够处理自然生物界面的动态和复杂的相互作用,并能够对干细胞疗法或植入设备等再生医学应用中的细胞-材料相互作用进行调节。
目前的发展
大多数关于生物应用响应表面的文献都集中于对外部提供的一种刺激作出响应的平坦、2D 表面。这些表面在细胞行为的动态控制方面已经显示出巨大的前景。然而,它们距离细胞和 ECM 之间发生的复杂相互作用还很远。在生物学中,多种刺激在复杂的 3D 结构中以动态且相互依赖的方式与细胞和 ECM 相互作用。在将其中一些方面纳入人工界面方面也取得了一些进展;这些进展将在这里回顾并在新一代生物界面的设计背景下进行讨论。
多重刺激响应材料
上面讨论的响应表面都被设计为响应一种刺激并提供一种预定响应。细胞与环境的自然相互作用要复杂得多,需要使用多种刺激和响应机制。单一响应的简化和隔离使我们能够设计在基本水平上模仿这些交互的表面;然而,它确实忽略了细胞与 ECM 相互作用的多重响应性质所产生的任何潜在的协同效应。为了推进人工细胞与材料的相互作用,有必要设计多刺激响应表面[ 5 ]。
多重刺激响应材料的概念正在成为响应材料界即将面临的挑战之一。近的一篇综述讨论了多响应聚合物的进展,并重点介绍了过去十年报道的许多多响应系统[ 133 ]。这些材料通常包含两种或更多种不同单体的嵌段聚合物或共聚物,其表现出对不同刺激的响应性。值得注意的是,可以设计将输入信号(初始刺激)转换为有意义的输出信号的多重响应表面。基于 pH 敏感的N , N-二甲基氨基丙基丙烯酰胺 (DMAPAM) 的三重刺激响应性无规共聚物,温度响应性N - t-丁基丙烯酰胺 (NTBAM) 和溶剂性敏感的 4- N -(2-丙烯酰氧基乙基) -N-甲基氨基-7- N , N-二甲基氨基磺酰基-2,1,3-苯并恶二唑 (DBD-AE) 显示荧光变化(光响应)由于 pH 值和温度引起的共聚物性的改变[ 134 ]。
原则上,多重刺激响应聚合物应该可转移到固体基底上以制备多重刺激响应表面。此类表面的报道很少。双刺激响应表面已通过表面引发聚合制备为 NIPAM(温度响应)和丙烯酸或甲基丙烯酸(pH 响应)的共聚物[ 115 , 116 ]。这些材料的特征在于润湿性[ 115 ]和溶胀特性[ 116 ],显示出这些特性随温度或pH值的变化。此类材料的生物学应用仍有待证明。
对生物环境中的多种刺激做出反应的表面具有明显的应用潜力,可以探索与更复杂的系统相互作用的协同效应。此外,设计具有多种响应的材料以更紧密地模仿 ECM 的多功能性也很有吸引力。例如,对多种刺激做出正交反应的多响应表面,对两种不同的刺激产生两种不同的反应,将使我们更接近于更复杂的细胞-材料相互作用。
3D 材料的响应表面
术语“3D 材料的表面”包括具有地形特征的材料的表面和多孔 3D 物体的内表面。两者在表面改性和表征方面都面临着重大挑战,但作为再生医学材料很受关注,因为它们除了呈现生物学相关的化学线索外,还提供了在一定程度上模仿 ECM 中存在的结构特征的环境。
也许,广泛使用的响应性 3D 材料是水凝胶,其刺激响应性降解已被用来调节网络结构 [ 71 ] 和弹性 [ 135 ] 以及化学功能的呈现 [ 135 ],从而能够控制细胞反应,例如细胞迁移[ 71 ]和分化[ 135 ]。由于这些是大量材料响应,我们不会在这里详细讨论它们。
固体 3D 支架广泛用作组织工程应用的支撑。修改此类 3D 结构的内表面对于创建同时模拟 ECM 的化学和结构动力学的响应式 3D 结构很有吸引力 [136 ]。实现这一目标的一个步骤是通过聚己内酯、聚乳酸或壳聚糖制成的聚合物基质中的生物降解来释放细菌包涵体[137 ]。尽管此示例依赖于降解,因此可能不完适合此处讨论的材料的特定刺激/响应相互作用,但它强调了解决多孔 3D 材料中表面响应性的可能性。
虽然存在多种 3D 材料的表面改性方法 [ 138-140 ],但内部 3D 结构的均匀表面改性并不简单,而且由于复杂 3D 结构表面分析的限制而变得更加复杂。这使得响应式 3D 表面的准备变得充满挑战。无标记化学 3D 分析 [ 141 , 142 ] 的新进展可能会解决其中一些问题,我们预计能够表征 3D 结构内表面的方法的出现将大大有助于制定能够设计3D 结构上的响应表面。
交互式生物界面
为了将人造材料完整合到生物环境中,材料不仅需要提供生物学相关的线索,而且能够对细胞呈现的生物刺激做出反应。在近的文献中,交互式和更复杂的细胞-材料界面的愿景,换句话说,以生物学相关的方式动态响应生物刺激的表面,已经开始出现[6, 13],并且已经设计了一些系统解决交互式生物界面设计的某些挑战。
为了将响应界面扩展到更加动态的、基于生物学的系统,细菌被用来修饰材料表面并产生作者所说的“活界面”,作为哺乳动物细胞和材料表面之间的中间体。非致病性细菌乳酸乳球菌经过基因改造,可表达含有纤连蛋白片段 FNIII 7-10 [ 143 ]的 RGD ,从而影响 C2C12 细胞的粘附和形态[ 144 ]]。虽然细菌修饰的表面并未显示出直接的细胞响应性,但我们可以想象细菌膜会对生物环境的变化做出响应,并且可能能够响应哺乳动物细胞引起的周围环境的变化表面上的文化。
表面对细胞提供的刺激的细胞响应已经通过采用代谢产物的形成作为触发事件来实现。乳酸乳球菌产生的乳酸会改变周围环境的 pH 值,从而影响 pH 响应表面的变化 [ 122 ]。pH诱导的聚丁二烯、聚(甲基丙烯酸)和季铵化聚(甲基丙烯酸2-(二甲氨基)乙酯)三嵌段共聚物的膨胀终导致细菌自诱导从表面脱离。
可以用细胞分泌的酶作为刺激来实现更有针对性的细胞诱导的表面反应。近利用能够充当碱性磷酸酶底物的肽表面探索了这种可能性[ 74 ]。侧翼为磷酸化丝氨酸和酪氨酸残基的 RGD 序列显示出对碱性磷酸酶的酶促去磷酸化反应敏感。在这些表面上培养间充质干细胞表明,细胞分泌的碱性磷酸酶可能能够诱导去磷酸化,而无需添加其他外部刺激,从而促进了细胞响应材料表面的概念。
细胞与材料相互作用的另一个新兴方面是与内部细胞过程的界面。细胞侵入技术已成熟用于测量膜电位等特性[ 145 ]。例如,通过使用基于碳纳米管的电化学传感器对细胞膜进行穿孔来测量细胞内参数[ 146 ],越来越引起人们的关注。研究表明,纳米尺寸的电可以无缝集成到细胞膜中[ 147 ]。因此,在表面上制造空心管(直径约 100 nm)并连接到储液器 [ 148]。这些管子被插入 HeLa 和中国仓鼠卵巢细胞中,结果表明荧光染料可以直接递送到细胞间隙中。将细胞内传感和细胞内材料输送相结合,可以预见,在不久的将来,一种能够实现细胞内细胞-材料界面的组合系统可能成为可能。
交互式生物界面在推进再生医学方面具有巨大潜力。更动态的组织培养平台将允许对体外进行更精细的控制细胞培养,能够制造具有更高复杂性和功能的更复杂的人造组织。细胞响应表面可用于监测生物过程,以设计传感器或更好地了解细胞如何与其环境和/或彼此相互作用。植入物上的动态响应表面不仅可以指导生物环境,还可以响应宿主组织的要求,从而更无缝地集成到宿主组织内。在各个方面都取得了有希望的进展,可能会使这项技术在不久的将来成为再生医学的强大工具,但在设计出真正可行的交互式生物界面之前,必须解决许多挑战。
结论与未来展望
旨在与生物环境交互的响应表面的终目标必须是提高人造材料与活细胞的整合水平。这种集成的性质可以采取多种形式,并且取决于生物界面设计的终应用。虽然在现有技术下,模仿生物学中存在的复杂而动态的相互作用,甚至部分地看起来可能是一项艰巨的任务,但它也提供了大量令人兴奋的机会。
识别响应界面的适当刺激至关重要,因为它决定了有关材料特性及其设计的后续考虑。人们已经探索了能够改变生物相关材料表面特性的各种刺激和材料反应。事实证明,光、电位、温度和 pH 值等更常用的刺激对于外部控制生物界面很有价值。
对于生物界面与生物环境的更紧密整合,生物分子的使用将有利,因为它们直接参与细胞过程的调节,因此可以用作调节细胞表面相互作用的标记和触发器。特别是,酶作为材料反应刺激物的使用正在迅速增加,并且随着对酶在生物过程和疾病状态中的相关性的了解不断增加,利用酶的催化特性作为材料表面和细胞之间的信使可能会变得有用。设计更无缝集成的生物界面。为此的一个重要先决条件是详细了解刺激酶在生物环境中的自然作用。
如果要将细胞与材料的相互作用转化为具有生物学意义的响应和适合实际生物医学应用的响应性生物界面,那么对生物刺激做出反应的表面设计将需要更多的关注。因此,有必要将针对散装材料开发的响应材料技术转化并扩展至生物界面。需要新的材料表面改性,不仅要响应生物分子(或其他刺激),还要将这种响应转化为表面或本体材料特性的可测量或功能变化。
迄今为止,仅使用有限数量的材料来制备用于生物应用的响应表面,从而可能限制了迄今为止观察到的细胞响应的类型。由于生物分子可能成为刺激响应生物界面设计的核心,因此可以预期,基于生物分子的表面由于其多功能性和与生物刺激相互作用的能力,在未来可能会引起越来越多的兴趣。
由于许多生物相互作用是可逆的,可逆响应生物界面的设计很可能利用类似的概念,例如,通过利用酶催化双向反应的能力,或利用两种不同的酶催化相反的反应。相同的基材。终,这一概念可能导致可逆生物界面的产生,其中一个或两个方向的变化可能依赖于燃料,例如,它们仅在存在其他辅因子的情况下发生。这种生物界面将代表向模仿生物过程的自然复杂性和多样性迈出的重要一步。
这些终有望导致更无缝的细胞-材料界面的产生,其中细胞不仅对来自表面的提示做出反应,而且表面也对细胞呈现的刺激做出反应。这种交互式生物界面对于自控或自主生物界面将有吸引力,并将开辟令人兴奋的应用潜力,以重建更复杂的细胞生态位,例如,干细胞的命运可以以前所未有的时间和空间方式控制,或者神经细胞可以在其中控制神经细胞的命运。可以与人造材料更无缝地连接。
出于实际原因,迄今为止,大多数生物界面都是在“平坦”基板上设计的,并且能够响应单一的外部提供的刺激。为了模拟生物系统的复杂性,需要对多种刺激做出反应,包括细胞提供的刺激和 3D 物体表面的修饰,并且已经开始出现应对这些挑战的策略。
近出现的允许进入细胞内环境的技术为在新水平上与细胞交互提供了令人兴奋的机会。虽然传统上细胞-材料界面从表面通过蛋白质层和整合素到达细胞骨架,从而影响细胞内过程,但材料与细胞内环境之间的直接相互作用将提供控制细胞行为并提供有关细胞内信息的新方法。流程。
设计这种复杂和动态的生物界面的一个主要挑战是它们的监测和分析。该领域的将在很大程度上依赖于合适的分析工具的可及性,这些工具能够在复杂的环境中(好是在活细胞存在的情况下)以高空间和时间分辨率监测细胞-材料界面。虽然表面和界面分析方面的新进展(例如对有机材料进行无标记 3D 表面分析的日益强大的能力)部分解决了这一挑战,但仍需要进一步的开发,以在对系统的干扰小的情况下获取生物界面的动态变化。
这里讨论的文献的新进展清楚地表明响应式界面的设计正在获得动力。关于响应性散装材料设计的文献已经广泛,并且响应性表面正在开发类似的工具集。基于该领域巨大的潜力和兴趣,我们可能会在不久的将来看到许多令人兴奋的发展,这些发展将大大推进人造材料与细胞的整合,并开辟大量新的应用。



























