英文名称: IdentiClone™ T and B-Cell Clonality Assays
T、B淋巴细胞基因重排检测
IdentiClone™ T and B-Cell Clonality Assays
【临床意义】
目前临床上多数以形态学表征,免疫表型来作为淋巴瘤分型的主要依据,然而很多淋巴瘤的表征是十分相似的,这类方法很难准确鉴别,容易导致误诊。分子诊断技术对于判断淋巴瘤具有独特的客观优势。淋巴瘤来源于淋巴细胞的恶变,恶变后仍然具有淋巴细胞的基本特征,即仍然有免疫球蛋白(Ig ,B细胞)或者T细胞受体(TCR T细胞)基因重排。PCR技术的兴起使得扩增Ig或者TCR基因变得很容易。标本来源包括血液,骨髓,组织和胸腹水,还可用于石蜡固定后的淋巴结标本。
【试剂盒原理】
PCR技术常被用来检测T细胞克隆性。本试剂盒引物扩增的DNA序列为保守的可变区(V)和链接区(J)间的序列及多变区和链接区间的序列。这些保守序列位于V-J区的两边,在B和T淋巴细胞成熟过程中,编码基因重排。B细胞中,抗原受体基因发生重排的是免疫球蛋白重链和轻链,T细胞中的T受体发生重排。每个B细胞和T细胞都有独特的V-J重排,重排产生单一的长度和序列。因此,当用DNA引物扩增正常的或多克隆群体的V-J区侧翼序列,在预期范围内,扩增产物形成一条钟型曲线(高斯分布)。聚丙烯酰胺电泳的产物则是弥散状条带。高斯分布反映了V-J重排的多样性。若DNA来自于克隆性样本,则在多克隆背景下会产生一个或两个明显的扩增产物。由于抗原受体基因的多态性(包含相关DNA序列的异质性群体),很难设计出一套引物可以把基因重排V-J区的侧翼序列全部包括在内,N区的多样性及体细胞突变更增加了该区段序列的多变性。因此,试剂盒设计了多管扩增Mix,定位多个FR区,旨在检测出绝大多数的基因重排。 在扩增结束后,可以通过聚丙烯酰胺电泳或毛细管电泳的方法,检测扩增片段的长度,来分析结果。
【产品优势】
² 唯一商品化试剂,获得CE认证,是细胞克隆性基因检测的“金标准”
² 检测方法多样,可通过聚丙烯凝胶电泳或ABI/毛细管电泳平台进行
² 产品性能稳定,样本来源可以是石蜡包埋组织或切片,外周血,组织块
² 基于PCR技术的克隆检测,改良的标准化流程
² 最丰富的阳性对照,涵盖T/B细胞重排类型
【试剂盒灵敏度分析】
InVivoScribe 公司的 IdentiClone™产品是基于PCR的克隆性检测产品。这些标准化的试剂的组分包括阴性对照,阳性对照,Mix 都是经过精心优化,产品经过了超过400例的临床样本验证,检测是在30多个从BIOMED-2合作组织中挑选出的优秀的独立实验室进行,实验结果发布在白血病领域的权威期刊Leukemia上。当所检测的克隆细胞群低于总体的5%时,凝胶电泳检测的方法所得到的结果可能不可靠。需要强调的是,克隆性检测的结果应与临床,病理及免疫学等方面的数据结合进行综合的判断。
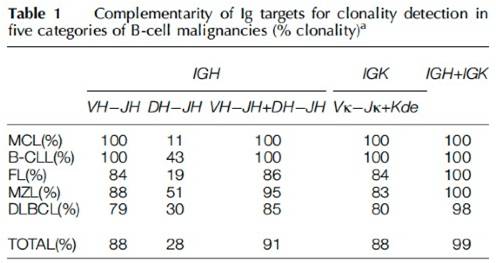
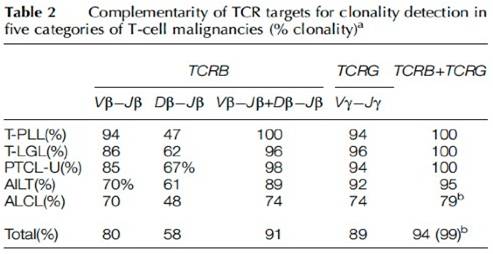
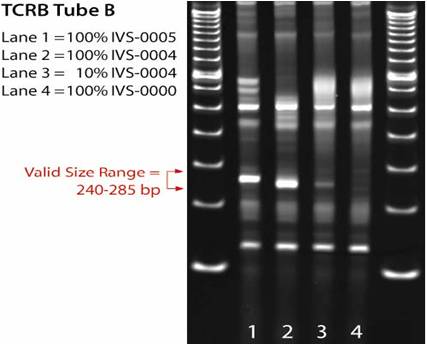
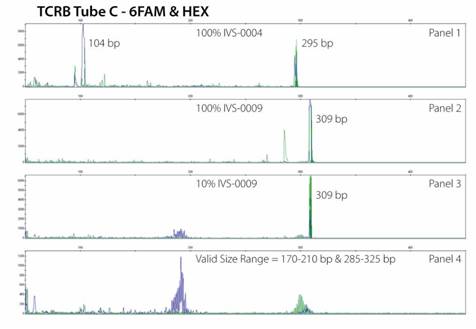
TCRB聚丙烯酰胺凝胶电泳图 TCRB毛细管管电泳Gene Scan图
订购信息
| 产品名称 | 货号 | 方法 | |
| TCRB克隆性检测试剂盒 TCRB克隆性检测试剂盒 TCRD克隆性检测试剂盒 TCRD克隆性检测试剂盒 TCRG克隆性检测试剂盒 TCRG克隆性检测试剂盒 TCRG克隆性检测试剂盒2.0 TCRB+TCRG克隆性检测试剂盒 TCRB+TCRG克隆性检测试剂盒 | 9-205-0010 9-205-0011 9-206-0020 9-206-0021 9-207-0020 9-207-0021 9-207-0101 9-200-0010 9-200-0011 | 电泳法 测序法 电泳法 测序法 电泳法 测序法 测序法 电泳法 测序法 |
| 产品名称 | 货号 | 方法 | |
| IgH克隆性检测试剂盒 IgH克隆性检测试剂盒IgK克隆性检测试剂盒 IgK克隆性检测试剂盒 IgL克隆性检测试剂盒 IgL克隆性检测试剂盒 IGH + IGK克隆性检测试剂盒 IGH + IGK克隆性检测试剂盒 | 9-101-0020 9-101-0021 9-102-0020 9-102-0021 9-103-0020 9-103-0021 9-100-0010 9-100-0011 | 电泳法 测序法 电泳法 测序法 电泳法 测序法 电泳法 测序法 |
| 产品名称 | 货号 | 方法 | |
| BCL-1/JH克隆性检测试剂盒 BCL-2/JH克隆性检测试剂盒 BCL-2/JH克隆性检测试剂盒 | 9-308-0010 9-309-0020 1-309-0051 | 电泳法测序法 电泳法
|
【相关文献索引】
1.Miller, JE, Wilson, SS, Jaye, DJ, Kronenberg, M. An automated semiquantitative B and T cell clonality assay. Mol. Diag. 1999, 4(2):101-117.
2.Van Dongen, JJM et al. Design and standardization of PCR primers and protocols for detection of clonal immunoglobulin and T-cell receptor gene recombinations in suspect lymphoproliferations: Report of the BIOMED-2 Concerted Action BMH4-CT98-3936. Leukemia 2003, 17(12):2257-2317.
3.Sandberg, Y, van Gastel-Mol, EJ, Verhaaf, B, Lam, KH, van Dongen, JJM, Langerak, AW. BIOMED-2 multiplex immunoglobulin/T-cell receptor polymerase chain reaction protocols can reliably replace Southern Blot analysis in routine clonality diagnostics. J. Mol. Diag. 2005, 7(4):495-503.
4.van Krieken, JHJM, et al. Improved reliability of lymphoma diagnostics via PCR-based clonality testing: report of the BIOMED-2 Concerted Action BHM4-CT98-3936. Leukemia 2007, 21(2):201-206.
【订购信息】